Користь від вакцини Pfizer для дітей переважує ризики - регулятор США
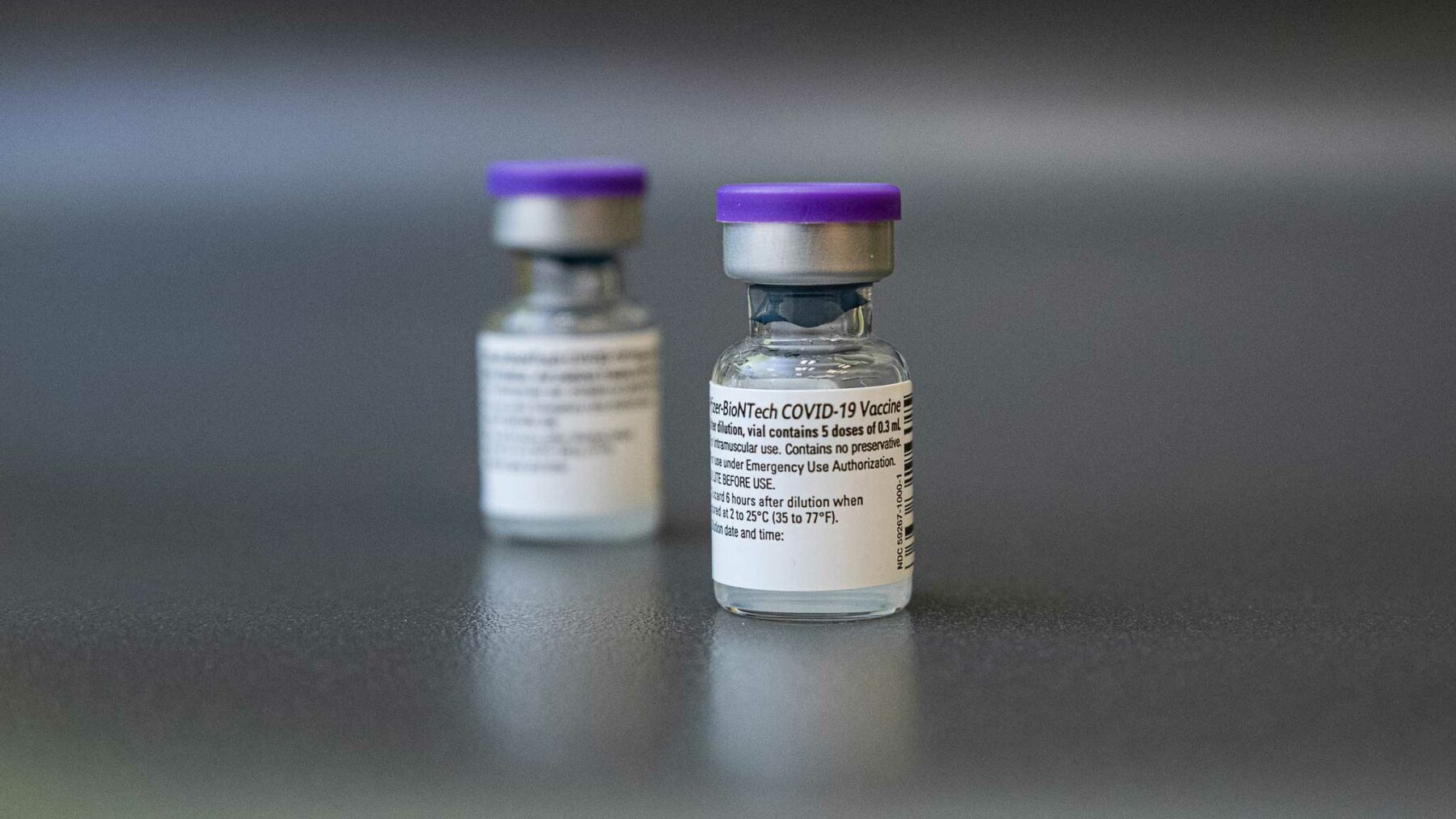
Раніше в п’ятницю виробники вакцин заявили, що їхня вакцина показала 90,7% ефективність проти коронавірусу в клінічному дослідженні дітей від 5 до 11 років. Подробиці були в брифінгу, опублікованому напередодні засідання групи зовнішніх експертів, яке має проголосувати у вівторок, чи рекомендувати FDA дозволяти вакцини для молодої вікової групи.
Якщо б FDA дозволила імунізацію Pfizer/BioNTech дітям від 5 до 11 років, це була б перша вакцина від COVID-19 для вікової групи, і щеплення можуть бути доступні у Сполучених Штатах на початку листопада.
Співробітники FDA сказали, що, припускаючи, що кількість випадків міокардиту, які спостерігаються у молодшій віковій групі, буде подібним до того, що спостерігається у віці від 12 до 15 років, кількість профілактичних госпіталізацій, пов'язаних з COVID-19, перевищить кількість госпіталізацій, пов'язаних з міокардитом, у більшості аналізованих сценаріїв. Pfizer припустив у своїх власних брифінгових документах, що частота міокардиту у віковій групі, ймовірно, буде нижчою, ніж у вакцинованих дітей віком від 12 до 15 років, частково тому, що дітям молодшого віку давали меншу дозу.
Шістнадцять дітей у дослідженні, які отримували плацебо, захворіли на COVID-19, проти трьох, які були вакциновані, повідомляє Pfizer в брифінгу, поданому до FDA. Оскільки у дослідженні з 2268 учасниками вакцину було введено більш ніж вдвічі більше дітей, ніж плацебо, це означає, що ефективність перевищує 90%.
На основі цих результатів Pfizer та BioNTech заявили минулого місяця, що їхня вакцина проти COVID-19 викликала у дітей стійку імунну відповідь. Співробітники FDA заявили, що вакцина відповідає критеріям агенції щодо імунної відповіді, яку вона викликала у дітей.
Анастасія Фаль - pravdatutnews.com